Rimoyt.com
Фазы и структурные составляющие железоуглеродистых сплавов
Основными компонентами, от которых зависит структура и свойства железоуглеродистых сплавов, являются железо и углерод. Чистое железо – металл серебристо-белого цвета с температурой плавления в 1539 °С. Железо имеет две полиморфные модификации: альфа () и гамма () . Модификация альфа существует при температурах ниже 911 °С и выше 1392 °С; гамма-железо – при температуре 911-1392 °С. В зависимости от температуры и концентрации углерода в железоуглеродистых сплавах (сталях и чугунах) образуются следующие твердые фазы: феррит, аустенит, цементит, графит.
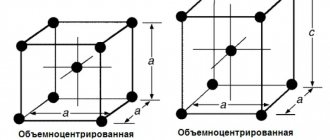
1. Феррит (Ф) – твердый раствор внедрения углерода в альфа-железе. Альфа-железо имеет ОЦК структуру, которая стабильна до 911 °С. Наибольшая растворимость углерода в альфа-железе – 0,02% при 727 °С. С понижением температуры снижается и растворимость углерода, и при комнатной температуре она составляет 0,005% по массе. По этой причине феррит называют технически чистым железом, он имеет незначительную твердость (HB = 80-100) и прочность (предел прочности в = 250 МПа), но высокую пластичность (относительное удлинение до 50%, относительное сужение до 80%). При температуре от 1392 °С до 1539 °С железо также имеет ОЦК структуру — это дельта-железо. Твердый раствор внедрения углерода в дельта-железе называют высокотемпературным ферритом.
2. Аустенит (А) – твердый раствор внедрения углерода в гамма-железе. Аустенит имеет ГЦК структуру. В железоуглеродистых сплавах аустенит может существовать только при высоких температурах. В гамма-железе углерод растворяется значительно лучше, чем в альфа-железе, максимальная растворимость углерода в гамма-железе составляет 2,14% и наблюдается при температуре 1147 °С. С пониженим температуры растворимость углерода снижается — до 0,8% при 727 °С. Аустенит имеет твердость HB = 160-200 и весьма пластичен (относительное удлинение 40-50%), наблюдается в сталях при температурах от 727 °С.
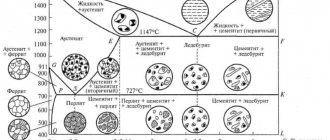
3. Цементит (Ц) – химическое соединение железа с углеродом (карбид железа Fe3C). В цементите содержится 6,67% углерода. Температура плавления цементита около 1600 °С. Он очень тверд (HB порядка 800 единиц), хрупок и практически не обладает пластичностью. Выделяют цементит первичный, вторичный и третичный. Их отличия заключаются в происхождении: — первичный цементит образуется из жидкого расплава при кристаллизации железоуглеродистых сплавов (линия СD), — вторичный цементит выпадает из аустенита (по причине уменьшения растворимости углерода в аустените с понижением температуры — линия SE) — третичный цементит выпадает из феррита с понижением температуры (по причине снижения растворимости углерода в феррите с понижением температуры — линия PQ) Цементит — неустойчивая метастабильная фаза. При нагреве и длительной выдержке цементит распадается на феррит (альфа-железо) и графит (Fe3C -> 3Fe + C).
4. Графит – чистый углерод с гексагональной слоистой структурой. Графит очень мягок (HB = 3) и обладает низкой прочностью. В чугунах и графитизированной стали содержится в виде включений различных форм (пластинчатой, хлопьевидной, шаровидной). С изменением формы графитовых включений меняются механические и технологические свойства сплава.
Помимо четырех вышеназванных фаз в струтуре сплавов железа с углеродом выделяют еще две самостоятельные структурные составляющие: перлит и ледебурит.
5. Перлит (П) – механическая смесь феррита и цементита, содержащая 0,8% углерода. Перлит образуется из аустенита при охлаждении его до температуры ниже 727 °С. Таким образом, перлит является эвтектоидом. Перлит может быть пластинчатым и зернистым (глобулярным), что зависит от формы цементита и определяет механические свойства перлита. При комнатной температуре зернистый перлит имеет предел прочности 800 МПа, относительное удлинение 15%, твердость HB = 160.
6. Ледебурит (Л) – механическая смесь аустенита и цементита (Л = А+ Ц), содержащая 4,3% углерода. Ледебурит образуется из жидкого расплава при температуре 1147 °С. Таким образом, ледебурит по своей сути является эвтектикой. Ледебурит образуется при затвердевании жидкого расплава при 1147 °С. Ледебурит имеет твердость HB = 600-700 HB и большую хрупкость. Ледебурит наблюдается в структуре чугунов, в сталях он образовывается только при большом количестве легирующих элементов и содержании углерода более 0,7%. При охлаждении ледебурита до температуры в 727 °С входящий в его состав аустенит становится неустойчивым и распадается, превращаясь в перлит. Таким образом, при температуре менее 727 °С вплоть до 20 °С ледебурит представляет собой механическую смесь перлита с цементитом.
| Феррит | Аустенит | Цементит | Графит | Перлит | Ледебурит | |
| Сущность | твердый раствор внедрения углерода в альфа-железе | твердый раствор внедрения углерода в гамма-железе | химическое соединение железа с углеродом | чистый углерод | механическая смесь феррита и цементита | механическая смесь аустенита и цементита |
| Обозначение | Ф или -Fe(C) | А или -Fe(C) | Ц или Fe3C | Г | П = Ф + Ц = Fe?(C) + Fe3C | Л = А + Ц = Fe?(C) + Fe3C |
| Твердость HB | 80-100 | 160-200 | 800 | 3 | 160 | 600-700 |
| Содержание углерода | до 0,02% | до 2,14% | 6,67% | 100% | 0,8% | 4,3% |
Фазы и структурные составляющие сплавов железа с углеродом
Помимо перечисленных структурных составляющих, в железоуглеродистых сплавах могут быть нежелательные неметаллические включения: окислы, нитриды, сульфиды, фосфиды – соединения с кислородом, азотом, серой и фосфором.
Теория сплавов
Чистые металлы относительно редко применяют в машиностроении, так как не обеспечивают необходимого комплекса механических и технологических свойств изготовляемых из них деталей. Широко используют сплавы, состоящие из двух и более элементов (из двух металлов, например меди и цинка, или из металла и неметалла, например железа и углерода).
Элементы, входящие в сплав, называют компонентами.
Сплавы получают сплавлением компонентов, спеканием, электролизом и возгонкой. Компоненты, входящие в сплав, в жидком состоянии почти всегда растворяются друг в друге, образуя жидкий раствор. Атомы такого раствора равномерно перемешаны друг с другом. Свойства сплавов зависят главным образом от взаимодействия компонентов при затвердевании. При затвердевании сплавов образуется твердый раствор, химическое соединение или механическая смесь.
Твердый раствор. При переходе в твердое состояние в сплавах сохраняется однородность распределения атомов различных компонентов, а следовательно и свойство растворимости. При кристаллизации сплава атомы компонентов входят в единую ячейку кристаллической решетки, поэтому получаются однородные и одинаковые по составу зерна. Твердый раствор, как и чистый металл, имеет однообразную кристаллическую решетку. В кристаллической решетке чистого металла все узлы заняты атомами одного компонента, а в решетке твердого раствора — атомами компонентов, составляющих сплав. В твердых растворах растворимость компонентов не ограничена при любом их количественном соотношении (медь с никелем).
Свойства сплавов, образующих твердые растворы, изменяются плавно и отличаются от свойств компонентов, из которых они стоят. Они отличаются ценными свойствами. Они тверже и прочнее, чем входящие в них компоненты, обладают хорошей пластичностью, высоким электросопротивлением, не изменяющимся при изменении температуры, повышенным сопротивлением к коррозии. Благодаря высокой пластичности такие сплавы хорошо обрабатываются давлением.
Химическое соединение. Компоненты некоторых сплавов при кристаллизации могут входить в химическую связь, образуя химическое соединение. Например, железо с углеродом образуют химическое соединение Fe3C — карбид железа (цементит); медь с магнием — Cu2Mg; магний со свинцом — Mg2Pb и др.
Химическое соединение, как и твердый раствор, обладает однородной структурой. Кристаллическая решетка его включает атомы обоих компонентов. Однако в кристаллической решетке химического соединения, в отличие от твердого раствора, атомы каждого компонента находятся в строго определенном количестве и расположены всегда одинаково. Например, химическое соединение железа с углеродом Fe3C всегда состоит из трех атомов железа и одного атома углерода, соединение Mg2Pb всегда имеет два атома магния и один атом свинца. Таким образом, химическое соединение имеет постоянный состав и выражается химической формулой, а состав твердых растворов изменяется в широких пределах, твердый раствор не может быть выражен химической формулой. Кристаллическая решетка химического соединения отличается от решеток входящих в него компонентов, поэтому при образовании сплава оно рассматривается как самостоятельный компонент. Например, сталь — сплав, одним компонентом которого является железо, а другим — химическое соединение Fe3C (цементит).
Химические соединения обладают очень высокой твердостью и хорошим электросопротивлением. Иногда их твердость в 10 раз превышает твердость чистых компонентов. Так, например, железо с углеродом образует химическое соединение Fe3C, твердость которого в 10 раз выше твердости железа. Химические соединения вольфрама и титана с углеродом (карбиды), отличающиеся очень высокой твердостью, используются для изготовления режущих инструментов. В отличие от твердых растворов химические соединения характеризуются высокой хрупкостью, для обработки давлением они непригодны.
Механическая смесь. Отдельные компоненты в твердом состоянии не растворяются друг в друге (с образованием твердого раствора) и не входят между собой в химическую реакцию (с образованием химического соединения). При кристаллизации у каждого из таких компонентов создается своя, свойственная только ему одному кристаллическая решетка. Перемешиваясь друг с другом при постоянной температуре и определенном процентном соотношении, они образуют механическую смесь, в которой при рассмотрении под микроскопом видны отдельные компоненты. Так, механическая смесь РЬ — Sb образуется при температуре 246°С и соотношении компонентов: РЬ -87%, Sb—13%.
Механические смеси имеют хорошие литейные свойства. Особенно это относится к эвтектическим сплавам, которые обладают большей жидкотекучестью и меньшей температурой плавления, чем составляющие их компоненты.
Знание строения сплавов облегчает их выбор при изготовлении деталей машин и разработке технологических процессов. При изучении процессов, происходящих в металлах и сплавах в случае изменения их температуры и состава, пользуются такими понятиями, как компонент, система, фаза.
Системой в термодинамике называют совокупность веществ или тел, между которыми может беспрепятственно проходить обмен энергией и массой. В качестве системы может выступать химический элемент (сера, алюминий, водород), химическое соединение (Fe3C, вода, поваренная соль), сплав двух и более металлов (медь- никель, олово — свинец — сурьма), водный раствор (сахар в воде), смесь газов (воздух, состоящий из азота, кислорода, углекислого газа и пяти инертны газов).
Фазой называется часть системы, имеющая однородное строение и отделенная от других частей поверхностью раздела. В состав фазы может входить любое число компонентов, из которых состоит система. Система может содержать одну фазу и более. Однокомпонентные системы «сера», «алюминий», «поваренная соль» при комнатной температуре имеют одну твердую фазу, система «вода» в этих же условиях содержит одну жидкую фазу, а система «водород» — одну газообразную фазу. При температурах ниже нуля система «вода» также однофазна, имеет одну твердую фазу — лед. При нуле градусов эта система двухфазна, так как при этой температуре сосуществуют жидкая (вода) и твердая (лед) фазы.
Двухкомпонентная система «раствор сахара в воде» — однофазная, т. е. имеет одну жидкую фазу, если раствор ненасыщенный. Эта же система будет двухфазной при насыщенном растворе, содержащем нерастворившиеся кристаллы сахара, которые являются второй (твердой) фазой. Жидкая фаза в данном случае будет содержать два компонента (воду и сахар), а твердая только один (сахар).
Промышленное получение
Железоуглеродистые сплавы производятся металлургическими заводами из разных компонентов. Основа — железо с углеродом. Этапы производственного процесса:
- Подготовка расходного сырья (руды). Ее сортируют по размерам кусков, химическому составу. Бедные руды обогащаются требуемыми компонентами. Пустые породы удаляются.
- Подготовка топлива. Коксовый уголь проходит процедуру грохочения. Она нужна, чтобы удалить из топлива посторонние примеси, которые могут привести к тепловым потерям при плавке руды.
- Подготовка флюса. Вещества, которые будет применяться для производства чугуна измельчают. При этом отсеивается мелочь, удаляются сторонние примеси.
- Загрузка расходных материалов, руды в доменную печь. Сначала она заполняется коксом, сверху выкладывается руда, поверх нее засыпается еще один слой кокса. Внутрь вдувается разогретый воздух для поддержания температуры плавления металла. При сгорании кокса выделяется большое количество углекислого газа, который проходит через остатки кокса, образуя соединение СО. В процессе восстановления железо набирается твердости. Постепенно углерод начинает растворяться. Жидкий чугун подается к специальным ковшам, из которых разливается по формам.
Для производства чугуна применяются большие доменные печи. Их высота может достигать 30 м, а внутренний диаметр — 12 м.
Доменная печь (Фото: Instagram / viktormacha)
Химические соединения
Основные структуры, составляющие железоуглеродистых сплавов:
Феррит представляет собой твердый раствор углерода в α-Fe. При температуре 723°C максимальное содержание углерода составляет 0.02%.It не вытравит если никакие примеси.
Цементит-соединение, содержащее углерод железа fe3c-6,67% карбида углерода. Эвтектика является неотъемлемой частью смеси и самостоятельным структурным компонентом. За счет замещения атомами других металлов может образовываться твердый раствор, который неустойчив и разлагается при термической обработке. Цементит очень твердых(НВ 800) и хрупок.
Аустенит представляет собой твердый раствор углерода в γ-Fe. Атомы углерода вводятся в кристаллическую решетку, и степень насыщения может варьироваться в зависимости от температуры и impurities. It устойчив только при высоких температурах, а стабилен даже при нормальных низких температурах-примеси Mn, Cr. Аустенитная твердость HB 170… 220.
Микроструктура:
- а-гиперэвтектоидная сталь-феррит (светлая область) и перлит (темная область) с увеличением 500X, б-эвтектоидная сталь-перлит (1000′), в-эвтектоидная сталь-зацепляющийся перлит и цементит (200’).)
- Растворимость углерода в феррите снижается с 727% при 0,02°с до 0,005% при комнатной температуре.
Свойства
Характеристики железоуглеродистых сплавов:
- Плотность — до 7,9 г/см3.
- Температура плавления — до 1520 °C.
- Удельная теплоемкость — 462 Дж/(кг·°C) при температуре окружающей среды не более 20 °C.
- Удельная теплота плавления — 84 кДж/кг.
- Коэффициент теплопроводности — 30 Вт/(м·К) при температуре 100 °С.
- Коэффициент линейного теплового расширения — 11,5·10-6 1/°C.
Железоуглеродистые сплавы производятся промышленными предприятиями. К ним относятся разные виды стали, чугуна. Они применяются в разных сферах промышленности.
Классификация
Сталь классифицируется по разным признакам. По химическому составу:
- Высокоуглеродистые — более 0,65% С.
- Среднеуглеродистые — от 0,25% до 0,65% С.
- Низкоуглеродистые — менее 0,25% С.
По структуре:
- заэвтектоидные;
- эвтектоидные;
- доэвтектоидные;
- ледебуритные.
По назначению:
- Инструментальные. Используются при изготовлении рабочих частей и оснастки электрических инструментов, промышленного оборудования.
- Конструкционные. Применяются при изготовлении металлоконструкций, деталей промышленного оборудования, машин.
Сталь в рулонах (Фото: Instagram / mmz_sim)
Сплавы железа с углеродом
Железоуглеродистые сплавы могут содержать следующие структурные компоненты:
- Феррит (F) представляет собой твердый раствор, содержащий углерод и другие элементы в iron. It имеет объемно-центрированную кубическую решетку. Растворимость углерода в феррите очень мала, до 0,005% при комнатной температуре. При 727°C, самая высокая растворимость 0,02% феррита очень пластична, мягка и обрабатывается путем приложения давления в холодных условиях.
Аустенит (а) представляет собой твердый раствор углерода и других элементов G-iron. It присутствует только при высоких температурах. максимальная растворимость углерода в г-железе составляет 1147% при температуре 2,14°С и 727 ° с при 0,8%.Эта температура является нижним пределом присутствия аустенита в железоуглеродистом сплаве. Аустенит очень пластичен, но тверже феррита.
Основные структуры
Сплав железа и углерода является основой стали и чугуна, которые называются железными сплавами, и это самые важные конструкционные материалы в технологии.
Структура и свойства сплава во многом зависят от характеристик основных компонентов и аддитивных элементов, а также характера их взаимодействия.
Чистое железо-серебристо-белый металл, тугоплавкий. Температура плавления железа составляет 1539°C. железо имеет 2 полиморфные модификации a и G.
- При температурах ниже 910°C железо имеет объемно-центрированную кубическую решетку. Это изменение называется A-iron. а-железо-это температура до 768°С (точка Кюри) магнитно.
Когда утюг нагрет, тел-центризованная кубическая решетка 910°С поворачивает в сторон-центризованную кубическую решетку, и А-утюг поворачивает в г-утюг. г-железо присутствует при температуре 910-1392°с
Углерод-неметаллический элемент. Температура плавления углерода составляет 3500°С. углерод в природе существует в 2 полиморфных модификациях: Алмаз и графит.
Форма алмаза не найдена в сплаве.
В сплаве свободный углерод-железо углерод находится в форме графита. Кристаллическая структура графита слоистая. Его прочность и пластичность очень низки.
Углерод может растворяться в железе в жидком и твердом состоянии, образуя химические соединения-цементит может находиться в свободной форме в виде графита.
Узловые критические точки диаграммы состояния системы железо углерод
На диаграмме железо углерод отмечено некоторое количество точек, называемых критичными. Каждая точка несет в себе информацию о температуре, долевом содержании углерода и описанием того, что именно происходит в этом месте.
Всего существует 14 этих критичных точек.
Например, А, говорит о том, что при температуре 1539 °С и при нулевом содержании углерода происходит плавление чистого железа. D говорит о том, что при температуре 1260 возможно плавление Fe3c.
Точки расположены на пересечении линий, размещенных на диаграмме.