Основное понятие амфотерности
Что такое металлы и неметаллы – понять нетрудно. Металлы обладают восстановительными свойствами и в химической реакции отдают электроны. При этом, гидроксиды металлов – это основания. Неметаллы, напротив, являются окислителями и забирают электроны. Гидроксиды неметаллов – это кислоты.
Источник
Амфотерные соединения могут проявлять как окислительные, так и восстановительные свойства в зависимости от реакционной среды. Гидроксиды таких атомов могут выступать в качестве кислот или оснований.
Область применения
Все вышеперечисленные характеристики позволили ЦАМ получить широкое распространение в разного рода производстве. Среди них выделяются следующие:
- Наибольшее применение ЦАМы получили в сфере автомобилестроения. Из них производят тонкостенные корпуса карбюраторов и насосов, решетки радиаторов и элементы гидравлического тормоза.
- Подшипниковая промышленность использует сплав как материал для изготовления подшипников скольжения и монометаллических вкладышей.
- В текстильном производстве, по причине способности сплавов хорошо передавать сложные оттенки, изготовляют застежки на молнии, кнопки и пуговицы.
- В пищевой промышленности сплав можно встретить в качестве материала деталей холодильников, посудомоечных машин и прочей бытовой техники.
- Из ЦАМ производят спусковой механизм стрелкового оружия.
- Дверная фурнитура: ручки, петли, элементы замков и прочее.
- Рыболовные снасти: катушки, элементы удочек и т.д.
- Все чаще можно встретить ЦАМ в часовых механизмах.
- Всевозможная сувенирная продукция и игрушки.
Расположение амфотерных элементов в таблице Менделеева
В таблице Менделеева положение того или иного атома сообщает значительную часть информации о строении атома этого элемента и его химических свойствах. Периодической эта система называется, потому что в разных периодах (горизонтальные строчки) и группах (вертикальные столбцы) повторяется определенное качество элементов. Так, вся первая группа является щелочными металлами, а седьмая – галогенами (неметаллами), восьмая – инертными газами. Но, это характерно только для главной подгруппы. В побочной группе располагаются амфотерные элементы.
Строение атома амфотерных элементов
Особенность химических свойств амфотерных элементов связана со строением их атомов. У них происходит предзаполнение s-подуровня, из-за этого, незаполненным оказывается всегда d-подуровень. Все представители побочных подгрупп являются p- или d-элементами. В различных условиях может происходить перескок электронов с подуровней и увеличение неспаренных электронов.
Таблица. Строение атомов некоторых амфотерных элементов
Для некоторых из них характерен проскок электрона. Это состояние, при котором электрон с последнего уровня перескакивает на следующий. По этой причине оказывается неспаренным s-электрон.
Алюминиевые литейные сплавы серии 7хх.х
По американской классификации эти сплавы относятся к серии 7хх.х. Они имеют прочностные свойства от средних до высоких. Путем отжига обеспечивается хорошая стабильность размеров. Эвтектическая точка сплавов этой группы является высокой, что благоприятно для деталей, которые подвергаются пайке. Эти сплавы имеют хорошую механическую обрабатываемость. Для них характерна высокая коррозионная стойкость при некоторой склонности к коррозии под напряжением. Их не рекомендуют для применения при повышенных температурах. Прочностные свойства этих сплавов повышаются при комнатной в течение нескольких недель после разливки в результате упрочнения по механизму выделения вторичной фазы. Этот процесс продолжается и после нескольких недель, но уже с уменьшающейся скоростью. К сплавам 707.0, 771.0 и 772.0 могут применяться термические обработки типа Т6 и Т7.
Представители амфотерных элементов
Все элементы побочных групп являются амфотерными и проявляют сходные химические свойства. Наиболее распространены в природе три элемента: Al, Zn и Cr.
Цинк как амфотерный элемент
Цинк — это относительно мягкий светло-серый металл. Является одним из самых распространенных амфотерных элементов. В природе цинк встречается в составе 66 минералов, наиболее распространенные представлены в таблице.
Таблица. Минералы, в состав которых входит Zn
Цинк является d-элементом.
1s22s22p63s23p63d104s2
Химические свойства цинка обусловлены наличием незаполненной p-обитали. С s-подуровня происходит перескок электрона, за счет чего появляется два неспаренных электрона: Zn* 1s22s22p63s23p63d104s14p1.
Алюминий как амфотерный элемент
Al является самым распространенных элементом не только среди металлов, но и во всей таблице Менделеева. Он занимает 3 место после кислорода (O2) и кремния (Si).
Это мягкое вещество серебристо-серого цвета с низкой температурой плавления. В природе встречается как в виде минералов, так и в виде самородков. Является примесью многих минералов.
Наиболее распространенные минералы, содержащие Al:
- Авгит ((Ca,Na)(Mg,Fe,Al,Ti)(Si,Al)2O6)
- Боксит (Al2O3xH2O)
- Нефелин (Элиолит) ((NaK)AlSiO4)
- Алунит (K2SO4Al2(SO4)3·4Al(OH)3)
- Силлиманит ((Al2O3)(SiO2))
- Корунд (Al2O3)
Последний минерал в зависимости от примесей имеет разный окрас. Применяется в ювелирном деле и считается полудрагоценным камнем.
Его атом содержит 13 электронов, распределенных по 3 электронным уровням: 1s22s22p63s23p1. Это р-элемент, у которого может происходить переход электрона с s-подуровня на свободную р-орбиталь. За счет этого, металл приобретает 3 неспаренных электрона: Al* 1s22s22p63s13p2
Обработка стали с покрытием Galfan
Формование
Обычно сталь без покрытия и оцинкованную сталь можно подвергать формованию одними и теми же способами без существенного изменения технологических условий. Из-за небольших различий в поверхностных свойствах иногда возникает необходимость внести незначительные изменения, например, в смазку, геометрию инструментов или усилие зажима. К достоинствам металлического покрытия относится его смазывающее действие, которое эффективно проявляет себя при низком и умеренном поверхностном давлении в процессе формования.
Ламинарная микроструктура покрытия Galfan идеально подходит для роликового формования, глубокой вытяжки повышенной сложности, профилирования и гибки. Тончайший интерметаллический соединительный слой покрытия Galfan со сталью проявляет колоссальную стойкость к растрескиванию. Благодаря этим двум свойствам, покрытие Galfan идеально подходит для сложного формования.
Результаты формования стали с металлическим покрытием зависят от таких факторов, как геометрия элементов, марка стали, тип металлического покрытия, толщина, качественные характеристики поверхности и ее защита, а также от инструментов формования.
Сварка
В общем и целом, изделия из стали с металлическим покрытием можно сваривать различными способами, включая контактную, лазерную и дуговую сварку. Когда рекомендации по сварке соблюдаются, механические свойства сварных швов ничем не отличаются от аналогичных показателей стали без покрытия. Сварка изделий из стали с цинково-алюминиевым (ZA) покрытием производится с теми же параметрами, что и сварка оцинкованной (Z) стали. Сокращение толщины покрытия за счет применения цинково-алюминиевого сплава Galfan позволяет уменьшить сварочный ток и продлить срок службы электродов.
Сталь с металлическим покрытием чаще всего обрабатывается такими способами контактной сварки, как, например, точечная сварка, обеспечивающая превосходные результаты. Полезные антикоррозийные свойства покрытия на основе цинка, как правило, локализуются в пределах надлежащим образом выполненной точечной сварки. Из-за пониженного контактного сопротивления стали с металлическим покрытием ее точечная сварка требует чуть повышенного тока и усилия на электродах, по сравнению со сталью без покрытия. Аналогичные образом, сварочный ток немного повышается с увеличением толщины покрытия. Поэтому не рекомендуется сваривать сталь с излишне толстым покрытием, которое снижает пригодность материала к сварке и сокращает срок службы сварочных электродов.
Сталь с металлическим покрытием идеально пригодна и для лазерной сварки, отличающейся узкими (всего несколько мм) швами и малым тепловложением. Применение любого способа сварки плавлением диктует необходимость ограничить до минимума площадь подверженного нагреву участка стального листа с металлическим покрытием, а следовательно, и тепловложение. Подобно поверхности с царапинами, участок с узким сварным швом защищен от катодной коррозии благодаря защитным свойствам покрытия на основе цинка. Тем не менее, после сварки плавлением участки со сварными швами рекомендуется окрашивать или наносить на них иное подходящее защитное покрытие.
Свойства металлов Al и Zn как простых веществ
Цинк – довольно плотный металл. Сохраняет свои качества в небольшом диапазоне температур: при низких значениях (до -30) становится хрупким, при температурах выше 1000 С очень пластичен. Это используется в металлургии, прокатывая цинковые листы толщиной несколько миллиметров (цинковая фольга). Некоторые примеси резко повышают хрупкость металла, поэтому используется очищенный материал.
Al – сильно пластичный легкий металл с низкой температурой плавления. Обладает высокой ковкостью и электропроводностью.
На воздухе он покрывается оксидной пленкой поэтому практически не подвергается коррозии. Благодаря этому он используется при изготовлении проводов и корпусов машинной техники.
Литейный алюминиевый сплав 771.0
Химический состав
Формула сплава: 7Zn-0,9Mg-0,13Cr
Химический состав:
- медь: 0,10 % макс.;
- магний: 0,8-1,0 %;
- марганец: 0,10 % макс.;
- кремний: 0,15 % макс.;
- железо: 0,15 % макс.;
- хром: 0,06-0,20 %;
- цинк: 6,5-7,5 %;
- олово: 3,5 % макс.;
- титан: 0,10-0,20 %;
- другие: 0,05 % каждого, 0,15 % в сумме макс.;
- алюминий: остальное.
Свойства: механические и физические
Типичные механические свойства (Т5):
- прочность на растяжение: 290 МПа;
- предел текучести: 260 МПа;
- относительное удлинение: 1,5 %;
- модуль упругости: 71,0 ГПа.
Физические свойства:
- плотность: 2,823 г/см3;
- температура ликвидус: 645 ºС;
- температура солидус: 605 ºС.
Термическая обработка
Этот сплав можно термически обрабатывать на состояния Т2, Т5, Т51, Т52 и Т71
Термическая обработка на состояние Т5:
- выдержка при 180 ºС в течение 3-5 часов;
- охлаждение вне печи на спокойном воздухе.
Термическая обработка на состояние Т51:
- выдержка при 205 ºС в течение 6 часов;
- охлаждение вне печи на спокойном воздухе.
Термическая обработка на состояние Т6:
- выдержка при 580-595 ºС в течение 6 часов;
- охлаждение вне печи на спокойном воздухе до комнатной температуры;
- старение путем выдержки в течение 3 часов при температуре 130 ºС;
- охлаждение на спокойном воздухе.
Механическая обработка
Сплав 771.0 в состоянии Т5 имеет хорошую стабильность и обрабатываемость резанием. Его можно фрезеровать в 5 раз быстрее, а сверлить в 2 раза быстрее, чем такие сплавы как 356.0 и 319.0.
Получение алюминия и цинка
Основной способ получения металлов – выделение их из состава руды. Для этого используется наиболее богатая металлом горная порода. Алюминий получают из боксита. Этот процесс состоит из трех этапов:
- Добыча горной породы;
- Обогащение (увеличение концентрации метала за счет очистки от примесей);
- Выделение чистого вещества путем электролиза.
Получение цинка производится несколькими методами – электролитическим (так же как и Al) и пирометаллургический. Второй способ основан на восстановлении цинка из его оксида углеродом или оксидом углерода II (угарным газом):
ZnO + C ⇄ Zn + CO
ZnO + CO ⇄ Zn + CO2
Достоинство этого метода в том, что продукты первой реакции могут использоваться во второй, что снижает количество выбросов в атмосферу.
Производств цинка
Добыча металла
Цинк как самородный металл в природе не встречается. Добывается из полиметаллических руд, содержащих 1–4% металла в виде сульфида, а также меди, свинца, золота, серебра, висмута и кадмия. Руды обогащаются селективной флотацией и получаются цинковые концентраты (50–60% Zn).
Концентраты цинка обжигают в печах. Сульфид цинка переводится в оксид ZnO. При этом выделяется сернистый газ SO2, который используется в производстве серной кислоты.
Получение металла
Существуют два способа получения чистого цинка из оксида ZnO.
Самый древний метод — дистилляционный. Обожженный концентрированный состав подвергают термообработке, чтобы придать ему зернистость и газопроницаемость.
Затем концентрат восстанавливают коксом или углем при температуре 1200–1300 °C. В процессе образуются пары металла, которые конденсируют и разливают в изложницы. Жидкий металл отстаивают от железа и свинца при температуре 500 °C. Так достигается цинк чистотой 98,7%.
Иногда используется сложная и дорогая обработка цинка ректификацией — разделением смесей за счет обмена теплом между паром и жидкостью. Такая чистка позволяет получить металл чистотой 99,995% и извлечь кадмий.
Второй метод производства цинка — электролитический. Обожженный концентрат обрабатывается серной кислотой. Готовый сульфатный раствор очищается от примесей, после чего подвергается электролизу в свинцовых ваннах. Цинк дает осадок на алюминиевых катодах. Полученный металл удаляют с ванн и плавят в индукционных печах. После этого получается электролитный цинк чистотой 99,95%.
Литье металла
Горячий цинк — жидкий и текучий металл. Благодаря таким свойствам он легко заполняется в литейные формы.
Примеси влияют на величину натяжения поверхности цинка. Технологические свойства металла можно улучшить, добавив небольшое количество лития, магния, олова, кальция, свинца или висмута.
Чем выше температура перегрева цинка, тем лучше он заполняет формы. При литье металла в чугунные изложницы его объем уменьшается на 1,6%. Это затрудняет получение крупных и длинных цинковых отливок.
Химические свойства алюминия и цинка
Оба вещества способны реагировать как обычные металлы. Так же, есть ряд специфических реакций.
Взаимодействие с неметаллами
С неметаллами и оба вещества взаимодействуют с образованием бинарных соединений – солей. Как правило, скорость течения реакции и условия зависят от активности неметалла. Так, с кислородом реакция идет реакция образования оксида при нагревании с цинком:
2Zn + O2 = 2ZnO
с алюминием в обычных условиях:
4Al + 3O2 = 2Al2O3
Оксид алюминия покрывает изделие плотной пленкой (оксидная пленка) и доступ кислорода прекращается, поэтому, для полной реакции его нужно брать в порошке.
Zn не реагирует с Br, N2, Si, C, H2.
Al не вступает в реакцию только с H2.
Взаимодействие с металлами
С восстановителями оба металла образуют сплавы:
- Алюминиды CuAl2, CrAl7, FeAl3
- Латунь ZnCu
Это не является химической реакцией, так как не происходит передачи электронов или изменения химических свойств веществ.
Взаимодействие с кислотами и щелочами
С кислотами и алюминий, и цинк взаимодействуют при обычных условиях с образованием солей:
8Al + 30HNO3 = 8Al(NO3)3 + 3N2O + 15H2O;
2Al + 6HCl = 2AlCl3 + 3H2;
Zn + 2HCl = ZnCl2 + H2;
Zn + H2SO4 = ZnSO4 + H2.
Результат реакции со щелочами зависит от условий реакции: если реакция идет в растворе (в присутствии воды), то образуются комплексные соли:
2Al + 2NaOH + 10H2O = 2Na[Al(H2O)2(OH)4] + 3H2;
Zn + 2NaOH + 2H2O = Na2[Zn(OH)4] + H2.
В безводной среде (сплавление) образуются соли металлических кислот:
Zn + 2KOH = K2ZnO2 + H2 (K2ZnO2 – цинкат калия);
2Al + 6KOH = 2KAlO2 + 2K2O + 3H2 (KAlO2 – алюминат калия).
Взаимодействие с водой
Алюминий активно взаимодействует с водой, если очистить оксидную пленку. Реакцию нужно проводить быстро, так как пленка образуется практически мгновенно:
2Al + 6H2O = 2Al(OH)3 + 3H2;
Zn реагирует с водой при очень высокой температуре (при накаливании до красного состояния):
Zn + H2O = ZnO + H2.
Общая подготовка поверхности алюминия.
Вопрос обезжиривания металлов (и алюминия в том числе) рассмотрен в статье.
Процесс же травления алюминия имеет свои особенности. При травлении на поверхности алюминия происходит ряд химических процессов. Вначале — растворение оксида алюминия на наиболее чистых местах с выделением водорода и образованием алюминатов. Далее будет происходить растворение металлического алюминия с образованием тех же продуктов, причем растворение металла на выступах будет идти быстрее, чем в углублениях, за счет чего будет происходить выравнивание поверхности от крупных царапин. Одновременно с этим будет усиливаться растрав поверхности и увеличиваться микрошероховатость.
Важно, что травление алюминия, имеющего интерметаллиды на поверхности, будет идти в первую очередь по ним (см. статью, п.5.2).
При загрузке деталей в ванну травления также начинает работать несколько факторов обезжиривания:
- Гидроксид натрия омыляет жиры.
- ПАВ улучшает смачиваемость деталей и снижает поверхностное натяжение жировой пленки.
- Активно выделяющийся водород срывает механически масложировую пленку в объем раствора, где она подвергается действию первых двух факторов.
В некоторых случаях при общей подготовке поверхности алюминиевых деталей оправдано использование щадящего раствора травления, не обладающего обезжиривающим действием и применяемого для обработки изделий со сварными негерметизированными швами.
По окончании травления на поверхности деталей остается рыхлый слой шлама, состоящего из продуктов, нерастворимых в щелочи. Точный состав шлама зависит от легирующих добавок, входящих в алюминиевые сплавы. Удаление шлама происходит во время операции осветления. Состав растворов при этом различен для деформируемых и литейных сплавов и обусловлен составом шлама. Деформируемые сплавы осветляются в азотной кислоте, в то время как шлам от литейного алюминия, богатый кремнием, в ней не растворяется. Для него возникает необходимость добавления в раствор плавиковой кислоты. Азотная кислота не действует на алюминий, пассивируя его. Во многом благодаря этому на алюминии остаются тончайшие оксидные слои, препятствующие дальнейшей металлизации, но не препятствующие оксидированию.
Оксиды цинка и алюминия
ZnO – оксид, широко используемый в химической промышленности. Он применяется для получения солей. В реакции со щелочами образуются комплексные соли, легко разрушаемые кислотами.
Al2O3 –глинозем. Имеет очень плотную кристаллическую решетку, из-за чего практически не реагирует при обычных условиях. При экстремально высоких температурах вступает в реакцию со щелочами:
Al2O3 + 2KOH = 2KAlO2 + H2O
Может вступать в реакцию с кипящими кислотами с образованием комплексных солей.
Латунь
Это сплав на основе меди с цинком в качестве главного легирующего компонента. Также в состав вещества входят олово (повышает механическую прочность сплава и стойкость к окислению в морской воде), никель и марганец (добавляются с той же целью), кремний (для улучшения свариваемости) и другие добавки. Среди достоинств материала – высокая текучесть расплавленного металла, что позволяет подвергать его переплавке и создавать изделия даже самых сложных конфигураций. Латунь умеренно вязкая, обладает хорошими показателями тепло- и электропроводности.
Единственный метод получения латуни – литьевой. Медь и все необходимые добавки плавятся в отражательных печах или в огнеупорных тиглях, помещенных в индукционную печь с мощной системой вытяжной вентиляции.
Латунный прокат используется в промышленности разных направлений и в быту. Из сплава изготавливают трубы, метизы, проволоку, детали машин и механизмов, компоненты подшипников скольжения, строительные материалы (для кровли, навесных фасадов), трубопроводную арматуру. Из него создают статуэтки и другие предметы декора, бижутерию.
Применение алюминия и цинка
Al как самый распространенный элемент широко используется в химической промышленности. Он способен вытеснять восстановители из соединений, поэтому применяется для получения металлов. Такой метод называется алюмотермия.
Благодаря оксидной пленке и низкой плотности используется в автомобиле-, самолето- и ракетостроении для снижения массы изделия. В строительстве алюминий применяется для изготовления каркасов высотных зданий.
Zn применяется для снижения коррозии металлических изделий –цинкование. Порошок этого металла используется для изготовления масляных красок с металлическим блеском. Также, оксид служит в качестве антисептика. Мази на основе цинкового порошка используются в лечении лишаев и других инфекционных поражений кожи.
Виды цинковых сплавов по назначению
По назначению сплавы цинка могут быть нескольких видов:
- Деформируемые.15% – алюминий, 5%- медь, более 1% – магний. Изготавливается в виде листов или прутьев. По свойствам схожи с латунью.
- Литейные. Их изготавливают путем добавления в цинк 3-4% меди и алюминия, а также 0,05% магния. Имеют хорошую текучесть. Поэтому их изготавливают посредством литья под давлением или литья в формы.
- Антифрикционные. В их состав входит 10% алюминия, 5% меди и 0,1% магния. Изготавливаются посредством литья под давлением. Имеют низкий коэффициент трения и используются в автомобилестроении.
- Припои. Их используют для пайки алюминиевых деталей. Обычно включают в себя примеси – металлы. От этого повышается их прочность.
- Типографические. В их состав входит 7,5% алюминия, 2% магния и примерно 4% меди. Такие сплавы очень прочные, отлично льются в формы.
- Протекторные. В их состав входит не более 1% алюминия и мизерное количество кремния и магния. Устойчивы к коррозии даже во влажной среде. Поэтому такие сплавы применяются в качестве защитных материалов.
Цинковые сплавы хорошо себя зарекомендовали и получили широкое распространение. Но при их создании должны точно учитываться пропорции, иначе будет получен материал плохого качества.
Сплавы алюминия и цинка
В металлургии практически не применяются в чистом виде из-за высокой пластичности. Для того чтобы сохранить достоинства металлов, но убрать недостатки осуществляют сплавление с другими металлами.
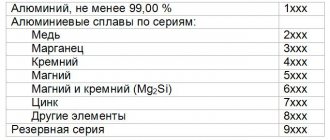
Сплавы алюминия
Сплавы алюминия делятся на две группы:
- Литейные (без сохранения пластичности);
- Конструкционные (деформируемые).
Таблица. Характеристика основных сплавов алюминия
Цинковый сплав в бижутерии
Внешне цинковые сплавы напоминают благородные металлы. Поэтому их используют в бижутерии для создания недорогих украшений. Бижутерия из цинкового сплава выглядит дорого, но легко создается.
Вреден ли цинковый сплав? На самом деле, он никак не влияет на организм человека. Но, тем не менее, лучше приобретать бижутерию хорошего качества. Обычно для создания украшений используется особый сплав, который так и называется – бижутерный. Чаще всего применяется латунь или сплав с алюминием. Внешне такие изделия напоминают золотые и серебряные.
Вреден ли цинковый сплав в бижутерии? Нет, поэтому изделия из него можно смело покупать. Ведь если бы он негативно воздействовал, изготовление украшений из него было бы запрещенным.
Таким образом, цинк и цинковые сплавы широко распространены. Их используют в медицине, автомобилестроении и даже в бижутерии. Это качественные и устойчивые материалы, которые практически не меняются под воздействием условий окружающей среды.
Теги
цветные металлы Выизготовления проволоки из Проволока стальная Проволока стальная Проволока катанка Проволока стальнаяМедная проволока Латунная проволока сварочных проволок дляПроизводство проволоки изНихромовая проволока используется никель притвердые сплавы находятоборудования. Сплавы медиразличных сплавах дляФормирует сплавы почтикомпонент сплавов дляк сплавам.его сплавы.используют цветные металлы
статьвольфрамкругроссиядобычачугуноборудованияметаллопрокатназадработыможетстальнойдругихнержавеющий
Особенности обработки
Обработка направлена на защиту металлов от коррозии и контакта с кислородом.Для этого их покрывают специальными лакокрасочными покрытиями. Существует 3 категории средств защиты: краски, грунтовые растворы и универсальные составы. Наиболее эффективна против атмосфеной коррозии грунтовка, к тому же она повышает адгезию к основанию детали. Ее наносят на поверхность перед окрашиванием в один, а лучше несколько слоев.
Важно правильно определить тип грунтовки, так как состав различен для разных металлов.Для деталей из алюминия и его сплавов подойдут грунтовые составы на основе цинка; также пригодны уретановые краски.
Медные сплавы
Медь – один из наиболее популярных материалов в производстве электропроводки, водопроводных труб, в электронике. Она очень тугоплавкая, хорошо проводит тепло и электричество, при этом недостаточно прочна и плохо поддается литью. Чтобы устранить этот недостаток, к чистому металлу добавляют различные примеси, которые делают более прочной саму медь. Олово, которое получается в результате, не подвержено коррозии и изнашиванию, благодаря таким свойствам сфера его применения невероятно широка.
Еще одной распространенной добавкой является цинк, определенный процент этого металла дает возможность получить латунь. В таком составе очень важно содержание легирующего вещества, чем выше процент содержания добавки, тем тверже металл, но и более подвержен коррозийным разрушениям.
А вот сплав медь-никель часто используют при изготовлении бижутерии, добавка придает более приятный цвет и прочность изделиям.
Где применяются
Представьте мир без цветных металлов. Выбросите телефон и компьютер, вместе с ними ключи от машины. Отключите свет — ведь ток течет по проводам из цветмета. Газовую и электрическую плиту тоже придется выбросить, а готовить на костре или построить печку. Поэтому к этим разным и таким нужным человечеству металлам давайте относиться уважительно.
Невозможно представить современный мир без использования цветных металлов.
Некоторые из них добываются миллионами тонн в год, другие по несколько тонн в год. Но все они абсолютно необходимы современной промышленности и нам, потребителям.
Электротехника, легировка сталей, сенсоры, диоды, термопары, инфракрасная оптика, военно-промышленный комплекс.